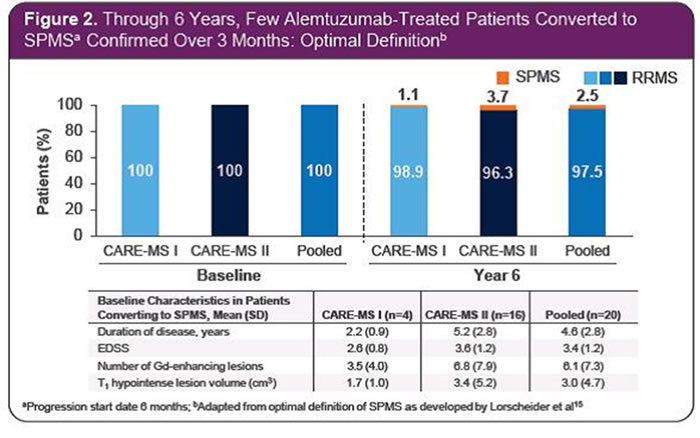
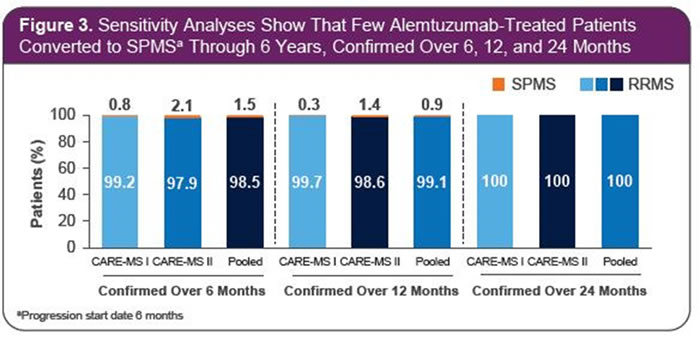
טיפול ב-Alemtuzumab (למטרדה) כקו ראשון או שני במטופלים עם טרשת נפוצה התקפית-הפוגתית הראה יעילות לטווח ארוך גם ללא טיפול מתמשך, ומציע לקלינאים ולמטופלים אפשרות חדישה לשליטה במחלה ולמניעת אובדן נפח מוח ונכות
Alemtuzumab (למטרדה – Lemtrada) הינו נוגדן אנושי המאושר לשימוש ביותר מ-50 מדינות. באיחוד האירופי, Alemtuzumab מאושר לטיפול במבוגרים עם טרשת נפוצה התקפית-הפוגתית עם מחלה פעילה, כפי שמוגדרת על ידי מאפיינים קליניים או מעבדתיים. בארה"ב, Alemtuzumab מאושר לטיפול במטופלים עם התקף טרשת נפוצה שהיו בעלי תגובה לא מספקת לשניים או יותר טיפולים משני מחלה (Disease modifying therapies).
במחקרים קליניים, Alemtuzumab הראה יעילות בטיפול במטופלים נאיביים לטיפולים קודמים עם טרשת נפוצה התקפית-הפוגתית פעילה, ובמטופלים עם חזרות לאחר טיפול קודם בטיפולים משני מחלה. האינדיקציות הנהוגות באיחוד האירופי מאפשרות לקלינאי גמישות משמעותית בנוגע להחלטות טיפוליות, המאפשרת לספק למטופלים רפואה מותאמת אישית.
Alemtuzumab עשוי להיות טיפול הבחירה במגוון רחב של מטופלים עם טרשת נפוצה התקפית הפוגתית, כולל, לדוגמה, מטופלים נאיביים לטיפולים קודמים עם מחלה פעילה, מטופלים עם מחלה פעילה מאוד או מטופלים עם התקפים למרות טיפולים משני מחלה קודמים.
ישנם מספר שיקולים שיש לקחת בחשבון כאשר מטפלים עם Alemtuzumab, לרבות צורת מתן ייחודית: מתן דרך הווריד למשך חמישה ימים עוקבים ולמשך 3 ימים עוקבים כ-12 חודשים לאחר מכן. במקרים מסוימים ולפי הצורך ניתן להוסיף מחזור טיפולי נוסף (3 ימים עוקבים לפחות 12 חודשים לאחר המנה האחרונה). בנוסף, נדרש ניטור חודשי קבוע למשך עד 48 חודשים לאחר המתן האחרון של העירוי על מנת לזהות בהקדם תופעות לוואי אוטואימוניות שעלולות להופיע.
בהינתן שיקולים אלו, חשוב להיחשף למידע אודות שימוש ב- Alemtuzumab בעולם האמיתי. לאחרונה פורסמו המלצות מצוות מומחים אירופאי לטרשת נפוצה לניהול המיטבי של טיפול ב-Alemtuzumab, כולל ניהול תופעות לוואי והיענות לדרישות ניטור מתמשך.
בהיעדר פרופיל מטופלים מסוים וביו מרקרים תקפים, ניסיון קליני מותאם אישית ישפיע בסופו של דבר על החלטות טיפוליות הקשורות ל-Alemtuzumab. ביחד, צוות המומחים האירופאי טיפל ב-181 מטופלים עם Alemtuzumab, כקו טיפול ראשון או, ברוב המקרים, כטיפול לאחר התקדמות המחלה על טיפול משנה מחלה קודם.
ישנה הסכמה, שתגובה טובה יותר לטיפול נצפית לרוב בטיפול בשלב מוקדם של המחלה, במטופלים צעירים, בעלי מחלה מאוד פעילה ורמה נמוכה של נכות התחלתית. עם זאת, בניסיון קליני, נמצא כי Alemtuzumab יעיל גם במטופלים עם נכות מצטברת, במיוחד כטיפול יעיל על מנת לייצב את המחלה ולמנוע החמרת הנכות כאשר יש פעילות דלקתית פעילה. לכן, המלצת צוות המומחים היא להשתמש ב-Alemtuzumab במטופלים עם טרשת נפוצה התקפית-הפוגתית, ללא קשר לרמת הנכות שלהם.
כ-15% מהמטופלים ייצגו קבוצה חשובה מאוד של מטופלים עם מחלה מוקדמת ופעילה מאוד. בהשוואה למטופלים שקיבלו טיפול עם Alemtuzumab בשלב מתקדם יותר, מטופלים אלו היו לרוב צעירים יותר, ועם מחלה קצרה ופעילה יותר, לרוב עם 2 או יותר התקפים ב-3-6 חודשים לפני הטיפול. צוות המומחים סבור, כי Alemtuzumab עשוי להיות אופציה טיפולית יעילה עבור מטופלים נאיביים לטיפול עם טרשת נפוצה מתפתחת במהירות (קלינית או הדמייתית), וככל שהניסיון יגדל והתוצאים החיוביים הקשורים עם טיפול מוקדם ב-Alemtuzumab יצטברו, שימוש ב- Alemtuzumab במטופלים אלו יגדל.
במחקר ה-CARE-MS Iי, Alemtuzumab הפחית משמעותית את שיעור האובדן המוחי במטופלים נאיביים לטיפול, ובהינתן קורלציה בין נפח אובדן מוח לנכות והחמרה קוגניטיבית, התערבות מוקדמת עם Alemtuzumab עשויה להיות מועדפת על פני דחיית הטיפול.
צוות המומחים סבור כי על פי הניסיון הקליני שהצטבר, ל-Alemtuzumab יש מקום בשימוש קליני שגרתי לטיפול במטופלים עם התקפים על טיפולים קודמים, כמו גם במטופלים נאיביים לטיפול. דחיית הטיפול ושמירת Alemtuzumab כמוצא אחרון איננה מומלצת, במיוחד עם מטופלים עם רמת נכות נמוכה, שטיפול בהם נמצא קשור עם שיפור נכות קיימת.
השאלה הגדולה העומדת בפני הקלינאים היא להחליט אילו מטופלים מתאימים לטיפול עם Alemtuzumab. בהינתן ההתוויה הרחבה לשימוש ב- Alemtuzumab באיחוד האירופי, קביעת פרופיל מטופלים מסוים עשוי להיות לא הכרחי, וייתכן אף לא אפשרי. למעשה, זה עשוי להיות יעיל יותר לקבוע אילו מטופלים אינם מתאימים לטיפול, כמו מטופלים עם מחלה לא פעילה, מטופלים יציבים עם הטיפול הנוכחי או מטופלים שלא יהיו מסוגלים להשלים את דרישות הניטור.
מטופלים מתאימים מחולקים לשתי קטגוריות: מטופלים נאיביים לטיפול ומטופלים עם תגובה חלקית לטיפול הנוכחי שלהם. Alemtuzumab עשוי לשמש כקו ראשון במטופלים נאיביים עם טרשת נפוצה פעילה, למרות ששימוש בתרופה עם פרופיל תועלת-סיכון כמו של Alemtuzumab בשלב מוקדם במחלה עשוי לדרוש שינוי תפיסתי אצל הקלינאים, באיזון בין הסיכון בהחמרת המחלה לסיכון שבטיפול.
בנוסף, היעילות של Alemtuzumab במטופלים עם מחלה פעילה מאוד מציעה שניתן להשתמש בו כטיפול במטופלים עם תגובה לא מספקת על הטיפול הנוכחי, או במטופלים שצריכים להחליף טיפול מסיבות שונות. למרות שישנם אתגרים לוגיסטיים הקשורים עם דרישות הניטור בקרב מטופלים המקבלים Alemtuzumab, ניתן לקזז זאת עם היעדר משטרי טיפול יומיים, שבועיים או חודשיים, בנוסף ליתרונות היעילות הניכרים שבטיפול.
בהינתן המהלך המורכב של טרשת נפוצה, עם מרכיב דלקתי ונוירו-דגנרטיבי, נראה שטיפול ב-Alemtuzumab יכול להשיג הפוגה קבועה בפעילות המחלה. Alemtuzumab מספק אפשרות טיפולית ייחודית עבור מטופלים עם טרשת נפוצה התקפית-הפוגתית, הכוללת יעילות עמידה גם ללא טיפול מתמשך, וכך מציע לקלינאים ולמטופלים אפשרות טיפול רחבה יותר לשליטה בטרשת הנפוצה.
ערכה: נועה יקריביץ'
מקור:
Thomas BergerEmail authorIrina ElovaaraSten FredriksonChris McGuiganLucia MoiolaKjell-Morten MyhrCelia Oreja-GuevaraIgor StoliarovUwe K. Zettl